
目次
化学の歴史
意外に知られていない化学の歴史。
だれが公式を作って定義したのか、いつ発見されたのか、そしてどのような恩恵を受けているのか。
まずはこのことを知っていないと化学は語れません。
日本史や世界史などと違い、年号まで暗記しなくてもよいですが、名前と法則くらいは知っておきましょう。
1744年 ラボアジェが「質量保存則」を定義しました。
ごくごく当たり前のことをいった法則で、「化学反応の前後で全質量は不変」というのが内容。
要するに、
ある教室に99人の生徒(男女比1:2)がいるとして、「男子一人と女子2人で手をつないで1つのグループを作ってください。」と言われたときに、果たして手をつなぐ前と後では生徒99人の体重の合計に変化があるでしょうか?
と聞かれれば「NO」と答えられる。
これが質量保存則。
昔は当たり前では無かったようです。
そして1799年にプルーストが「定比例の法則」を導きだし、そしてこの2つの法則から、1803年にドルトンが「原子説」を唱えました。
この原子説、当時の人々からしてみれば到底受け入れがたいものでした…
ここで歴史の話をしてもいいのですが、何も面白くないので次に大事な法則を紹介します。
そしてこの原子説を踏まえ、1811年にアボガドロが「分子説」を唱えたのです。
大きく分けてこの4つが時代背景にあり、そして仮説が何十年もさきに証明されていくのです。
残念ながらすべての法則の定義を解きほぐすことはしないのでそれぞれで調べてみると面白いかもしれません。
>>1ヶ月で早稲田慶應・難関国公立の英語長文がスラスラ読めるようになる方法はこちら
理論化学の大事なところ
結論から言ってしまえばすべて大切。
化学を勉強する上で、理論化学というものは化学という括りのなかで基幹(基礎をなすもの)となる分野です。
結合、構造、化学式、原子構造、イオン、結晶、酸塩基、中和滴定。キリがありません。
が、しかしこの中で「何が重要なのか」と聞かれれば「全部」と答えるしかありません。
なぜか。
理論を理解していないと無機で取り返しのつかないことになってしまうのです。
ですので以下には基幹の基幹にあたる部分、導出部分を重点的に説明させていただきます。
>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
理論化学の大事なところ①物質量
いわゆる理論、有機、無機化学の根底にあたる部分。
そもそも理論化学において勉強していった先にあるものは無機化学です。
「そもそも物質量もわからないで化学勉強できるわけないでしょ」というのが本音です。
さて、その物質量とはなんなのか。
教科書などには「化学式Xで表される粒子Xの相対質量に…」なんて長ったらしく書いてあり、思わず読むことをやめてしまいましたが、簡単に説明するとすれば物質量は「日本円」と言うことです。
ここからはたとえ話として
…1万円のお買い物をしたとしましょう。
さて、1万円をだしてください。と言われたときに、1円玉を1万枚出した日には威力業務妨害で捕まってしまいかねません。
なので1万円を1円玉で出す人なんていないんです。
そもそも、1つの粒子の中にどれくらいの重さの物が入っているかなんて誰にも分らないんです。
1円玉1万枚のおもさを知ってるひとが世の中に何人いるかと言われても、そうそういないわけですからね。
だからこそ、その膨大な数を「1つの文字でおこう」と言って1万円、つまり1㏖に置き換えられたのが「物質量」なのです。
ここでアボガドロ定数( 6.02×10²³個/㏖)が生まれた、ということです。
ですがやはり、海外旅行なんかしてみたいものです。
そこで必要になるのが「両替」という行為。
受験ではこの両替が自由自在にできなければ、まったくもって歯が立ちません。
ですので自分の頭の中で両替所を作ってください。
さて、両替してみましょう。
まずアメリカに行きたいとなれば「ドル」に変えなければなりません。
ここでは「粒子の個数」としましょう。
さて、1万円(以下㏖)をドルに換えたいとき、必ず「アボガドロ定数をかける」ことが必要になります。
先ほど説明した通り、2㏖あれば粒子の個数は1㏖の2倍。
当然ですが2×1㏖( 6.02×10²³個/㏖)です。
これでめでたく「両替」が完了しました。
同じようにして物質量から質量、気体の体積、個体・液体の体積(質量経由で両替)に変換できます。
ここは公式として覚えなければなりません。
さて、一通り旅が終わり帰国の準備に入ります。
海外旅行は行ったきりというわけにもいかないので、帰国しましょう。
ですが通貨はまだ多国籍の物のまま。ではどうするのか。
この分野のポイントとしては各通貨の「単位」を合わせることです。
先ほどの2㏖を個数に変換するときの動作を続けると、(2㏖)×アボガドロ定数(6.02×10²³個/㏖)ですね。
ここで単位に注目すれば、㏖×個/㏖になっています。
アボガドロ定数の単位は個数を㏖で割ったものなので、㏖が相殺されて「個」だけが残ります。
そしてめでたく「個数(ドル)」がえられたわけです。
帰国の際は「行きと逆」のことをすればOK。
つまり、アボガドロ定数を割れば「物質量(㏖)」に戻るという仕組み。
両替の際に発生する条件は、問題を多くやるうちに覚えてくるので、早めに定着させましょう。
ここさえ押さえてしまえば、物質量と付随するほかの体積や個数までも覚えられます。
なるべくいろいろな関係を見出して記憶する作業にはいれば、量も少なく済みますし、効率もグンとあがります。
理論化学の大事なところ②結晶
結晶には大きく4種類あります。
「イオン結晶」「分子結晶」「共有結合結晶」「金属結晶」。
たった4つなのに大事な理由。
それはこの分野を理解しなければ「試験問題文」の図が分からなくなってしまうこと。
そのなかの金属結晶にも構造があり、「面心立方格子」「体心立方格子」「六方細密構造」があります。
並の私立大学ならその構造内部の原子数や半径、構造名を「受験」で出す大学もあるくらいです。
学校の期末テストならまだしも、受験で出してしまうのは少しやりすぎな気もしますが、解けない人は多いんです。
間違っても受験本番で導出しようなんて愚かな考えをする人はいないとは思いますがね。
それぞれの構造については必須知識になるので必ず覚えましょう。
さて4つの結晶についてです、まずイオン結晶。
この結晶の大きな特徴といえば「硬くてモロイ」ことです。
矛盾しているようなことを言っていますが、イオン結晶とはその名の通り「陽イオンと陰イオンが結合してできた結晶」です。
ではなぜ硬いのにもろいのか。それは陽と陰で結合しているため、1つ結合がずれてしまうと「すべての陽と陰の結合が反発しあって、叩いたりすると割れてしまう」からなのです。
なので硬いのですが、もろいんです。
次に金属結晶。
言わずもがな金属原子同士の結合結晶です。
特徴は柔らかいものから硬いものがあり、電気をよく通して展性、延性があること。
そしてなんといっても「叩いても割れたりしない」ことですね。家庭のフライパンを使って料理をしていたら割れてしまった!なんてことないですね。
そしてフライパンといえば、熱しやすく冷めやすい。これも金属結晶の性質のひとつです。性質や構造はどんなに頑張っても式では表せないので、これも必須知識として覚えるほかありません。
続いて共有結合結晶。
なんといっても有名なものはダイアモンド。
瞬間的な力には弱いものの、とにかく電気陰性度が大きく、そして硬い。
ここで一つ、差が付くポイント。
「ダイアモンドには融点や沸点は存在するのでしょうか」。
答えは「条件下による」です。
1気圧の場合、4237℃で気体炭素になるということ。
厳密に100倍気圧にしたときには液体は存在するかもしれませんが、以上のことは熱している途中でダイアモンドが燃えてしまわない、真空中のなか前提。条件が変われば結果はわかりませんね。
そして最後に分子結晶。
この結晶は他の結晶と違い、分子式で表します。(他は組成式)
代表例は一番身近な「氷」や「ドライアイス」。
分子結晶は分子間力(ファンデルワールス力)によって規則正しく並んでいる結晶のこと。
特徴は沸点、融点がともに低い事、そしてもろく、昇華しやすい点にあります。
ドライアイスをたとえに使いましょう。
よくケーキなんかを買うとつけてくれたりしましたが、水に入れて遊んでいた記憶があります。
水に入れると「ブクブクして湯気?のようなものが出る」ことを知っていたのでやっていましたが、ただドライアイスを常温下に置いておいただけなのにドライアイスがなくなっている、なんてことがありました。
それはCO₂(個体)→ドライアイスの昇華点がマイナス温度だからなのです。
なので個体から液体の手順を踏まずにいきなり気体になって飛んで行ってしまいます。
もっとわかりやすい例でいえば、熱々に熱したフライパンの上に(危険なので真似は厳禁)氷を乗せると一瞬で水蒸気になってしまいます。
こちらのほうが想像しやすいかと思います。
ちなみにドライアイスに水をかけると湯気?が出てきますが、実は水蒸気なのです。
気になったら一度調べてみてもいいかもしれませんね。
理論化学の大事なところ③気体
高校生では決して落としてはいけない分野の一つ。
化学の中で一番コスパの良い分野でもあります。
どういうことかというと、覚えるべきことはただ一つ。
気体の状態方程式( PV=nRT)のみ。
なんといってもセンター試験や国立、私立2次試験に多く出題される分野です。
しかし、1つの式を知っていれば解ける問題を10分や20分もかけて完答できない受験生は多くいます。
なぜなのかは置いておいて、把握すべき状況が分かっていないことが多いです。
ここの分野で意識すべき点は「何が一定なのか、どこが変化しているのか、グラフを使って解ける問題なのか」ということ。
進度が進んでいくと「熱化学」という分野があり、この分野では特殊な「勝手に反応させてしまう」という高等テクニックがありますが、何事にも基本から入るべきですので、間違っても特殊な方法で解こうなんて考えないようにしましょう。
具体的には問題ごとにグラフを書いてみることが一番なのですが、最初は読み取ることもままならない受験生がおおいので、まず状況をしっかり把握することが大切。
センター試験なんてものは本来30分以内で終わらせなければならないのですが…多くの問題の場合、一回問題を見ただで「温度、圧力、体積」のどれかが分かります。
センターは特に後は計算だけ、なんて問題が多いので30分以内に解けます。
発展的に「温度一定に保ち、圧力を…」なんて文言が多いことも事実ですが、反応前と後で状態方程式を立てるだけに変わりはありません。
この分野で点を落してしまうのは「計算ミス」か「よほど意地の悪い問題」かのどちらかでしょう。
なので難関国立(東京一工、旧帝大)や難関私立(早慶上智理科大)を受験するひとは確実に得点源にします。
だからこそ「大事なところ」なんです。たかだか気体の分野で…なんて思うかもしれませんが、ここで落としてしまっては面白くもなんともないです。
他のひとが取れている分野で落としてしまったら勝負にもなりませんからね。
ですので気体は「戦略的」に大事なところになります。
理論化学のおすすめの参考書&問題集
「鎌田の理論化学の講義」と言う参考書は、基本事項の理解と問題演習の両方ができます。
センター試験で8割以上を狙えるようになるでしょう。
理論化学がニガテな受験生にも、ぴったりの参考書です。
理論化学の勉強法まとめ
勿論これ以上に大事な分野は多くあります。
が、今回紹介したことは0から何かを2にするのではなく、0から1へ、1から2へと着実にフォローアップするためのメソッドです。
公式や文言にとらわれずに「化学的」に問題も見て取れるようになったことでしょう。
⇒1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら
現役の時に偏差値40ほど、日東駒専に全落ちした私。
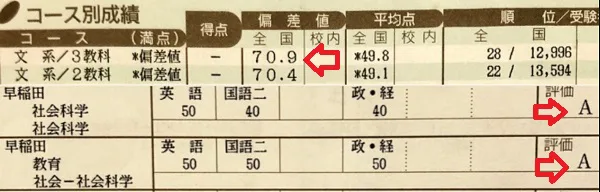
しかし浪人して1ヶ月で「英語長文」を徹底的に攻略して、英語の偏差値が70を越え、早稲田大学に合格できました!
私の英語長文の読み方をぜひ「マネ」してみてください!
・1ヶ月で一気に英語の偏差値を伸ばしてみたい
・英語長文をスラスラ読めるようになりたい
・無料で勉強法を教わりたい
こんな思いがある人は、下のラインアカウントを追加してください!
筆者は現役時代、偏差値40ほどで日東駒専を含む12回の受験、全てに不合格。
原因は「英語長文が全く読めなかったこと」で、英語の大部分を失点してしまったから。
浪人をして英語長文の読み方を研究すると、1ヶ月で偏差値は70を超え、最終的に早稲田大学に合格。
「1ヶ月で英語長文がスラスラ読める方法」を指導中。
⇒【秘密のワザ】1ヵ月で英語の偏差値が40から70に伸びた方法はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら











