

>>1ヶ月で早稲田慶應・難関国公立の英語長文がスラスラ読めるようになる方法はこちら

記事と筆者の信頼性
・難関大学に化学受験で合格した人が記事を執筆
・早稲田大学卒の予備校講師が、さらに分かりやすく編集
・編集者は予備校講師として、2,000人以上の受験生を指導
イオン式とは?
そもそも、イオンとは何なのでしょうか。
百科事典には下のように書かれていますが、分かりづらいですよね。
「中性の原子,原子団または分子が1個または数個の電子を失うか,逆に過剰の電子を得て電荷をもつ状態になったもの。電子を失ったものは正電荷を帯びて陽イオン (カチオン) となり,電子を得たものは負電荷を帯びて陰イオン (アニオン) となる。その電気量は電気素量の整数倍で,その倍数をイオンの電荷数という。電荷数は周期表における元素の族と関係している。たとえばアルカリ金属は電荷数+1のイオンに,ハロゲンは電荷数-1のイオンとなる。イオンは電解質溶液中やイオン結晶の中に存在する。気体の場合は,放電やX線,電子,陽子などの放射線照射によって生成する。イオンは元素記号の右肩にイオン価と電荷の符号をつけ,Na+ ,Fe3+ ,または Cl- のように表現する。
引用:https://kotobank.jp/word/%E3%82%A4%E3%82%AA%E3%83%B3-29970

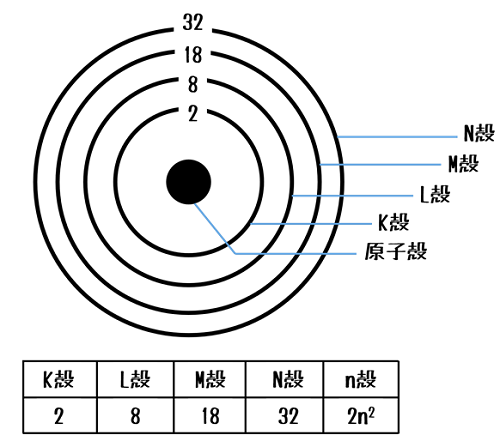
簡易的な原子を見ると、原子核を中心に電子殻がK殻からL、M・・・と構成されています。
そしてそれぞれの充てんできる電子の数は決まっています。
K殻2個、L殻は8個・・・となっています。
充填される電子の数が元素の種類を特徴づけています。
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
希ガスは超安定!
その中で、希ガスと呼ばれるグループ(周期表では列のことを示していて、族といいます)の電子配置で最も安定しています。
「希ガスの状態が一番安定している」ことはとても大切なので、忘れないようにしましょう!
下の図をご覧ください。
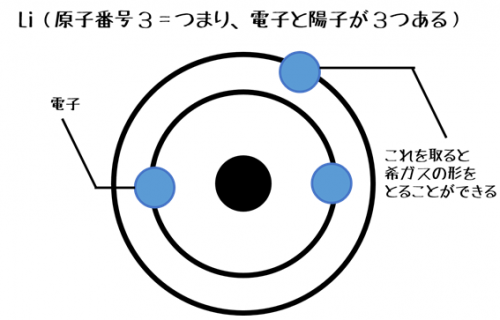
例えばリチウムLiについて、どんな原子も安定した希ガスの電子配置を取りたがります。
しかし電子を何個も抜いたり足したりするのは、大変な作業です。
ですから電子の足し引きが少ない手順で、希ガスの電子配置を取るように仕事をします。
Liの場合、一番外側の1つの電子を取ることで、ヘリウムHeと同じ電子2個の状態になります。
Liは本来電子3個ですが、1個の電子を引き抜くことで電子が2個になり、Heと同じ電子配置の状態になっています。
この状態をイオンと言います。
電子を抜き取ったとき「抜き取った数+正の符号」。
Liでは、Li+と書き、リチウムイオンといい、陽イオンと総称されます。
電子を加えたとき「抜き取った数+負の符号」となります。
一般的な原子では、「陽子の数=電子の数」です。
イオンでは、「陽子の数>電子の数」または「陽子の数<電子の数」となります。
>>1ヶ月で早稲田慶應・難関国公立の英語長文がスラスラ読めるようになる方法はこちら
イオン式をもっと詳しく解説します!

イオンになったとき、化学式の右肩に価数と符号を書きます。
ちなみに1価(1つの電子を抜いたり、足したりする)の場合は符号のみで表します。
イオンを表した化学式をイオン式と言います。
イオン式の作り方は簡単なんですが、受験に向けて覚えるのはそれなりに大変です。
イオン式の名称の解説
陽イオンについては「“元素名”+“イオン”」です。
H+の時には「水素イオン」、陰イオンについては「元素名から“素”という字を引く+“化物イオン“」となり、S2-と表します。
ただし例外が多いので、気を付けて覚えなければいけません!
命名の法則性とよく出るイオン式を表にまとめたので、ぜひ参考にしてください。
| 価数 | 名称 | イオン式 |
| 1 | 水素イオン | H+ |
| 1 | リチウムイオン | Li+ |
| 1 | ナトリウムイオン | Na+ |
| 1 | カリウムイオン | K+ |
| 1 | ルビジウムイオン | Rb+ |
| 2 | ベリリウムイオン | Be2+ |
| 2 | マグネシウムイオン | Mg2+ |
| 2 | カルシウムイオン | Ca2+ |
| 2 | ストロンチウムイオン | Sr2+ |
| 2 | バリウムイオン | Ba2+ |
| 2 | 亜鉛イオン | Zn2+ |
| 3 | アルミニウムイオン | Al3+ |
| 2 | 鉛(Ⅱ)イオン | Pb2+ |
| 3 | クロム(Ⅲ)イオン | Cr3+ |
| 2 | マンガン(Ⅱ)イオン | Mn2+ |
| 2 | 鉄(Ⅱ)イオン | Fe2+ |
| 3 | 鉄(Ⅲ)イオン | Fe3+ |
| 2 | ニッケル(Ⅱ)イオン | Ni2+ |
| 2 | 銅(Ⅱ)イオン | Cu2+ |
| 1 | 銀イオン | Ag+ |
| 2 | 酸化物イオン | O2ー |
| 2 | 硫化物イオン | S2ー |
| 1 | フッ化物イオン | Fー |
| 1 | 塩化物イオン | Clー |
| 1 | 臭化物イオン | Brー |
| 1 | ヨウ化物イオン | Iー |
| 1 | 水酸化物イオン | OHー |
| 1 | シアン化物イオン | CNー |
| 2 | 炭酸イオン | CO32ー |
| 1 | 炭酸水素イオン | HCO3ー |
| 1 | 酢酸イオン | CH3COOー |
| 2 | シュウ酸イオン | C2O42ー |
| 1 | 硝酸イオン | NO3ー |
| 2 | 硫酸イオン | SO42ー |
| 2 | 亜硫酸イオン | SO32ー |
| 1 | 硫酸水素イオン | HSO4ー |
| 3 | リン酸イオン | PO43ー |
| 1 | チオシアン酸イオン | SCNー |
ここで注目してほしいのが「金属イオン」。
金属の価数は色々あって覚えるのが面倒くさそうですが、覚えることは意外に少ないです。
ここで一度おさらいしてみましょう。
まず遷移元素で複数価数を持つ金属は、「カッコの中に価数を書く」。
そして「数字はローマ数字を書く」ことが決められています。
酸化銅(I)や酸化銅(II)というようになります。

>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
イオン式①1価の金属
アルカリ金属Na+、 K+、etc.
銀Ag+
これだけです!
イオン式②3価の金属
鉄Fe3+(2価も有り)
アルミニウムAl3+
これだけ。

イオン式③2価の金属
金属の価数は圧倒的に2価が多いです。
アルカリ土類金属Mg2+、 Ca2+、 Ba2+
亜鉛Zn2+
銅Cu2+
鉄Fe2+
鉛Pb2+
ニッケルNi2+
マンガンMn2+
スズSn2+
イオン式④その他
クロムCr6+、Cr3+
銅Cu+ (普通は2価)
水銀Hg+、Hg2+
スズSn4+
Cr6+、Cr3+の補足
クロム酸は酸性にしても、塩基性にしても6価のままです。
ただし酸性で還元剤があれば、6価のクロムが3価になります。
「さおに秋」
さ・・・酸性
お・・・オレンジ
に・・・二クロム酸
あ・・・アルカリ性
き・・・黄色
と何度も口に出して覚えておきましょう!
>>偏差値が1ヵ月で40から70に!私が実践した「たった1つのワザ」はこちら
イオン式⑤銅
1価の銅に関しては、ヨウ化銅(I)とフェーリング反応に使われれる酸化銅(I)あたりしか出てきません。
難しいことは考えず、とりあえず覚えちゃいましょう。
イオン式⑥マンガン
Mnは酸化還元反応では、赤紫色のMn7+(過酸化マンガン)から淡赤のMn2+(マンガン(II)イオン)になります。
ここで注意してほしいのは、「Mn自体が反応する場合に価数が変化する」という点。
M4+(二酸化マンガン)からM2+(塩化マンガン)への化学反応も価数変化の問題で有名だと思います。
マンガンは触媒にも広く使われていますが、触媒の場合はそれ自体が反応しませんので、価数も変わりません。
ちなみにアルカリ金属、アルカリ土類金属、亜鉛、アルミニウム、水銀は典型元素です。
他は全て遷移元素です。
>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
周期表を使った覚え方のコツ!

1価の陽イオン
1価の陽イオンになるのは、水素と1族のアルカリ金属です。
H ・ Li ・ Na ・ K ・ Rb ・ Cs ・ Fr
覚え方「Hなリナちゃんカルビくすねてフランスへ」
2価の陽イオン
2価の陽イオンになるのは、2族のアルカリ土類金属です。
Be ・ Mg ・ Ca ・ Sr ・ Ba ・ Ra
覚え方「便利なマグからストロー、バラ」
1価の陰イオン
1価の陰イオンになるのは、17族のハロゲンです。
F ・ Cl ・ Br ・ I ・ At
覚え方「ふっくらシュウマイいいいあした」
2価の陰イオン
2価の陰イオンになるのは、16族のカルコゲンです。
O ・ S ・ Se ・ Te ・ Po
覚え方「押す、背、鉄砲」

>>1ヶ月で早稲田慶應・難関国公立の英語長文がスラスラ読めるようになる方法はこちら
イオン式の暗記のポイント

金属イオンは複数の価数を持つことがありますが、基本的に2価です。
「2価でないもの」覚えることで、効率的に攻略できます。
陽イオンについては「“元素名”+“イオン”」です。
H+の時には「水素イオン」、陰イオンについては「元素名から“素”という字を引く+“化物イオン“」となります。
複数価数ある場合、カッコ付けで、ローマ数字で価数を書きます。
>>1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
補足:イオンの色

せっかくなので、イオンの色についても覚えてしまいましょう。
Fe2+・・・淡緑色
Cr3+・・・暗緑色
Fe3+・・・黄褐色
CrO42-・・・黄色
Cu2+・・・青色
Cr2O72-・・・赤橙色
Mn2+・・・淡赤色
MnO4-・・・赤紫色
⇒1ヵ月で英語の偏差値が40から70に伸びた「秘密のワザ」はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら
現役の時に偏差値40ほど、日東駒専に全落ちした私。
しかし浪人して1ヶ月で「英語長文」を徹底的に攻略して、英語の偏差値が70を越え、早稲田大学に合格できました!
私の英語長文の読み方をぜひ「マネ」してみてください!
・1ヶ月で一気に英語の偏差値を伸ばしてみたい
・英語長文をスラスラ読めるようになりたい
・無料で勉強法を教わりたい
こんな思いがある人は、下のラインアカウントを追加してください!
筆者は現役時代、偏差値40ほどで日東駒専を含む12回の受験、全てに不合格。
原因は「英語長文が全く読めなかったこと」で、英語の大部分を失点してしまったから。
浪人をして英語長文の読み方を研究すると、1ヶ月で偏差値は70を超え、最終的に早稲田大学に合格。
「1ヶ月で英語長文がスラスラ読める方法」を指導中。
⇒【秘密のワザ】1ヵ月で英語の偏差値が40から70に伸びた方法はこちら
⇒【1カ月で】早慶・国公立の英語長文がスラスラ読める勉強法はこちら
⇒【速読】英語長文を読むスピードを速く、試験時間を5分余らせる方法はこちら











